¿Cuál es el alimento para las plantas?
A diferencia de los animales que se alimentan de materia orgánica, las plantas se alimentan de materia inorgánica. La absorción de los elementos químicos se produce fundamentalmente a través de sus hojas y a través de sus raíces. Del aire toman el carbono y el oxígeno que se encuentran combinados formando el dióxido de carbono (CO2). El proceso de fotosíntesis es capaz, con la ayuda de la luz solar, de convertir este compuesto junto con el agua y los minerales tomados del suelo en azúcares. Carbono, oxígeno e hidrógeno constituyen los nutrientes no minerales.
¿Cómo mejorar un suelo deficiente en sales?
Cuanto más tarde un suelo en eliminar el agua, menor será su contenido en oxígeno durante ese tiempo. Si el suelo permanece saturado de agua por mucho tiempo, las raíces se asfixian y la planta crecerá raquítica, enfermiza y al final muere. Por supuesto, también está la posibilidad de mejorar el suelo de determinados sectores, en los cuales deseamos colocar plantas con menor resistencia. Un cambio parcial de éste, incorporando tierra arenosa en ese lugar, resuelve el problema, siempre y cuando el drenaje sea eficiente.
¿Cómo se obtienen las sales?
Son compuestos resultantes de la combinación de un metal con otro elemento no metálico o con un radical ácido, y que se consideran como producidas por sustitución del hidrógeno de los ácidos por átomos metálicos. Las s. resultan, pues, de la sustitución de uno o más átomos de hidrógeno de un ácido por átomos metálicos o radicales electropositivos. La s. común, de la que se deriva este nombre genérico, es el cloruro sódico, CINa, en cuya fórmula el sodio (v.) ocupa el lugar del hidrógeno del ácido clorhídrico (v. III). Otros ejemplos de s. son el sulfato cúprico, S04Cu, en el que el cobre (v.) ha sustituido al hidrógeno del ácido sulfúrico, S04H2, o el nitrato potásico, N03K, en el cual el hidrógeno del ácido nítrico ha sido reemplazado por el potasio (v.). Algunas s. contienen radicales en lugar de átomos metálicos, como el cloruro amónico, CINH4
Enalce Químico
Un enlace químico es el proceso físico responsable de las interacciones atractivas entre átomos y moléculas, y que confiere estabilidad a los compuestos químicos diatómicos y poliatómicos. La explicación de tales fuerzas atractivas es un área compleja que está descrita por las leyes de la electrodinámica cuántica.[1] Sin embargo, en la práctica, los químicos suelen apoyarse en la mecánica cuántica o en descripciones cualitativas que son menos rigurosas, pero más sencillas en su descripción del enlace químico. En general, el enlace químico fuerte está asociado con la compartición o transferencia de electrones entre los átomos participantes. Las moléculas, cristales, y gases diatómicos -o sea la mayor parte del ambiente físico que nos rodea- está unido por enlaces químicos, que determinan la estructura de la materia.
Los enlaces varían ampliamente en su fuerza. Generalmente, el enlace covalente y el enlace iónico suelen ser descritos como "fuertes", mientras que el enlace de hidrógeno y las fuerzas de Van der Waals son consideradas como "débiles".
Iónico
El sodio y el [cloro] uniéndose iónicamente para formar cloruro de sodio.]]
En [química], el enlace iónico es una unión que resulta de la presencia de atracción electrostática entre los iones de distinto signo, es decir, uno fuertemente electropositivo (baja energía de ionización) y otro fuertemente electronegativo (alta afinidad electrónica). Eso se da cuando en el enlace, uno de los átomos capta electrones del otro.
Dado que los elementos implicados tienen elevadas diferencias de electronegatividad, este enlace suele darse entre un compuesto metálico y uno no metálico. Se produce una transferencia electrónica total de un átomo a otro formándose iones de diferente signo. El metal dona uno o más electrones formando iones con carga positiva o cationes con una configuración electrónica estable. Estos electrones luego ingresan en el no metal, originando un ion cargado negativamente o anión, que también tiene configuración electrónica estable. Son estables pues ambos, según la regla del octeto adquieren 8 electrones en su capa más exterior. La atracción electrostática entre los iones de carga opuesta causa que se unan y formen un compuesto.
Los compuestos iónicos forman redes cristalinas constituidas por iones de carga opuesta, unidos por fuerzas electrostáticas. Este tipo de atracción determina las propiedades observadas. Si la atracción electrostática es fuerte, se forman sólidos cristalinos de elevado punto de fusión e insolubles en agua; si la atracción es menor, como en el caso del NaCl, el punto de fusión también es menor y, en general, son solubles en agua e insolubles en líquidos apolares como el benceno.
Ión
Un ion, también escrito ión,[1] (‘el que va’, en griego; siendo ἰών [ión] el participio presente del verbo ienai: ‘ir’) es una partícula cargada eléctricamente constituida por un átomo o molécula que no es eléctricamente neutra. Conceptualmente esto se puede entender como que, a partir de un estado neutro de un átomo o partícula, se han ganado o perdido electrones; este fenómeno se conoce como ionización.
Los iones cargados negativamente, producidos por haber mas electrones que protones, se conocen como aniones (que son atraídos por el ánodo) y los cargados positivamente, consecuencia de una pérdida de electrones, se conocen como cationes (los que son atraídos por el cátodo).
Anión
Un anión es un ion con carga eléctrica negativa, es decir, que ha ganado electrones. Los aniones se describen con un estado de oxidación negativo.
Catión
Un catión es un ion ( sea átomo o molécula) con carga eléctrica positiva, es decir, ha perdido electrones. Los cationes se describen con un estado de oxidación positivo.
Las sales típicamente están formadas por cationes y aniones (aunque el enlace nunca es puramente iónico, siempre hay una contribución covalente).
ACTIVIDADES DE LABORATORIO
Martes. 08 Febrero

Obtención de sales.
Material: tres tubos de ensaye, gradilla de hierro, pipeta.
Sustancias: Acido clorhídrico, acido sulfúrico, acido nítrico, hidróxido de sodio, hidróxido de potasio, hidróxido de calcio.
Procedimiento:
- Colocar dos ml del acido en un tubo de ensaye, adicionarle tres gotas del indicador universal y observar y anotar los cambios.
- En otro tubo de ensaye, colocar dos ml, del hidróxido y adicionarle, tres gotas del indicador universal.
- En el tercer tubo mezclar las dos mezclas de los tubos anteriores
OBSERVACIONES:
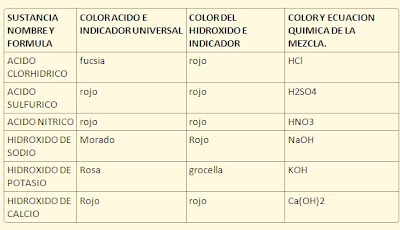

Material

Producto
Jueves. 11 Febrero
El enlace químico

♥Enlaces químicos♥
Material: Probador de conductividad eléctrica, capsula de porcelana.
Sustancias: Agua destilada, Laminas de: aluminio, magnesio, cobre, cloruro de calcio, sacarosa, carbón.
Procedimiento:
- Colocar una muestra de cada sustancia en la capsula de porcelana, cuidadosamente probar su conductividad eléctrica, anotar los resultados en el cuadro de observaciones:

Conclusiones:
En general los metales son buenos conductores de la corriente eléctrica y presentan enlace metálico, a diferencia del agua, al carbón y la sacarosa no conducen la corriente eléctrica por tener enlace covalente y polar.

Probando conductividad eléctrica

Conductividad eléctrica de algunas frutas
Viernes. 11 Febrero
Recapitulación 5. Quinta Semana
Equipo 1
El día martes 8 revisamos varios temas como: ¿Cuál es el alimento para las plantas?, ¿Cómo se mejora un suelo deficiente en sales? Y ¿Cómo se obtienen las sales?, y por ultimo realizamos una practica para mostrar como se obtienen las sales.
El día jueves 10 revisamos el tema de enlaces químicos, y realizamos una practica con varias sustancias para ver si tenían o no conductividad, y que tipo de enlace tenían estas.
Laura.Saludos.Buen trabajo.Favor de incluir la Bibliografía de las indagaciones y texto a las fotos.Quedan registradas.Gracias.
ResponderEliminarProf. Agustín